10 月 11 日,在第二十九届长城国际心脏病学会议上,长沙市第三医院心血管内科张育民教授就《抗栓治疗与消化道损伤的预防处理》进行了分享。
张教授指出,在抗栓治疗中,我们往往要关注其带来的另一面,即出血,而消化道是抗栓治疗最常见的并发出血部位,所占的比例最大。对于消化道损伤的预防和处理是临床医生应该重视和掌握的。

抗血小板药物致消化道损伤的特点
发生时间: 服药后 12 个月内为多发阶段,3 个月时达高峰。
与剂量的关系:在一定范围内,ASA 的抗血栓作用并不随剂量增加而增加。
与剂型的关系:尚无 ASA 泡腾片或肠溶片较平片明显降低消化道损伤危险证据。
与年龄的关系:老年患者是高危人群,年龄越大,危险越大。
与 HP 感染关系:HP 感染加重 ASA 的消化道损伤作用,开始长期治疗前,建议检测并根除 HP。
联合用药:抗血小板药物联合应用或与抗凝药物联用使上消化道出血的风险增加 2-7 倍。
损伤机制
阿司匹林致消化道损伤的机制
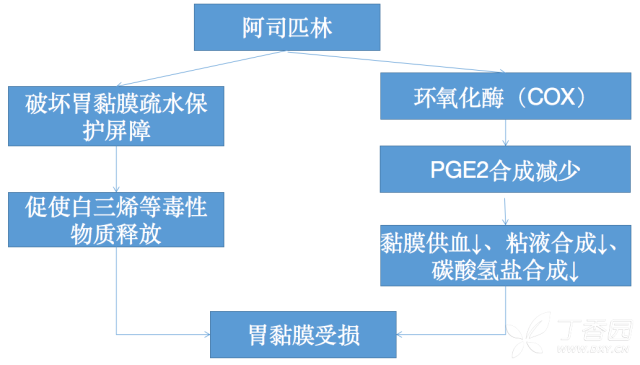
氯吡格雷致消化道损伤的机制
与阿司匹林不同,氯吡格雷并不直接损伤消化道粘膜
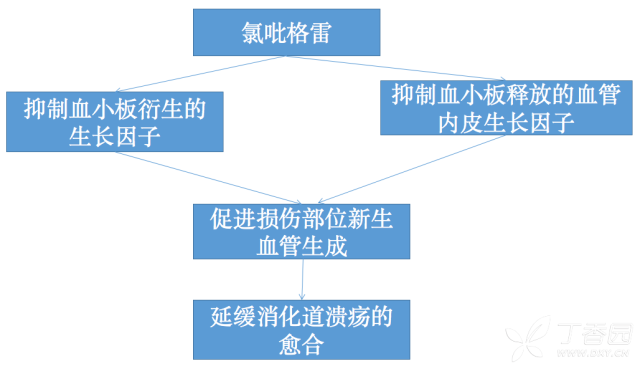
ACS 预防消化道出血的诊治策略
临床风险评估
选择合适的双抗时程
识别消化道损伤高危人群
抗栓治疗策略的调整
选择合适 PPI 进行防治
出血的非药物处理
1.临床风险评估
2011 ESCUA/NSTE-ACS 指南强调同时评估缺血与出血风险
缺血风险评估:继续强调 GRACE 评分作为评价缺血风险的有利工具(ⅠB)
出血风险评估:首次推荐 CRUSADE 评分作为评价院内外出血风险的工具,建议医生广泛使用(ⅠB)。CRUSADE 出血危险评分越高,患者的出血风险越高。CRUSADE>30 的出血中高危患者死亡风险较无出血患者升高 2~3 倍
2.选择合适的双抗时程
2017 年欧洲最新 DAPT 指南
(1)对行 PCI 的稳定性冠心病患者建议如下
植入支架者,无论支架类型,通常推荐 ASA+氯吡格雷双抗 6 个月(I,A)
高出血风险者(PRECISE-DAPT ≥ 25),应考虑双抗 3 个月(Ⅱa,B)
药物球囊扩张者,应考虑 6 个月双抗治疗(Ⅱa,级)
能耐受 DAPT 未发生出血事件者、出血风险低而缺血风险高者,可考虑延长双抗 6~30 个月(Ⅱb,A)
担忧 3 个月双抗的安全性者,可考虑 1 个月双抗(Ⅱb,C)
(2)对行 PCI 的 ACS 患者建议如下
植入支架者,推荐在 ASA 基础上加用一种 P2Y12 抑制剂双抗 12 个月,除非出血风险高(例如:PRECISE-DAPT ≥ 25)(I,A)
植入支架者,若出血风险高(例如:PRECISE-DAPT ≥ 25),可考虑在双抗 6 个月后停用 P2Y12 抑制剂(Ⅱa,B)
耐受双抗无出血事件者,可考虑延长双抗至 12 个月以上(Ⅱb,A)
ACS 特珠人群抗血小板治疗的中国专家建议
对近期消化道出血病史患者抗血小板治疗的临床推荐如下
具有高危消化道出血风险的 ACS 者(包括老年人、服用华法林、糖皮质激素或者 NSAIDs 等),推荐在氯吡格雷和阿司匹林 DAPT 基础上服用 PPI。
既往有消化道出血史的 ACS 患者进行抗血小板治疗时应联合应用 PPI 3~6 个月,其后可考虑继续或间断服用 PPI。
DAPT 期间发生消化道出血的患者,如必须停用一种抗血小板药物,则首先停用阿司匹林,必要时停用两种抗血小板药物。病情稳定后,3~5 天恢复氯吡格雷,5~7 天后恢复阿司匹林。
服用替格瑞洛发生消化道出血的患者,出血稳定后,可换用氯吡格雷维持治疗。必要时可联用 PPI,首选泮托拉唑,其次为埃索美拉唑、雷贝拉唑、兰索拉唑、奥美拉唑。
3. 识别消化道损伤高危人群
年龄大于 65 岁的老年人
既往消化道疾病的患者
双联抗血小板治疗的患者
合用抗凝药的患者
合用 NSAIDs 或糖皮质激素的患者
HP 感染、吸烟、饮酒等
(1)消化道损伤风险评估和筛查流程
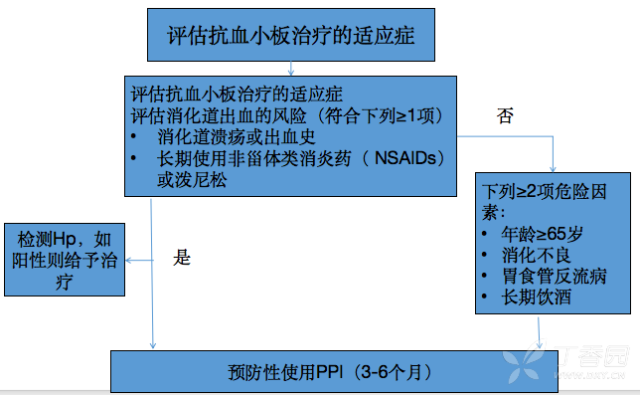
(2)上消化道出血评估
建议对所有急性上消化道出血患者进行 Blatchford 评分,以便在内镜检查前预判哪些患者需要接受输血、内镜检查或手术等干预措施,其取值范围为 0-23 分,0-6 分为低危组,>6 分为高危组。
Blatchford 评分
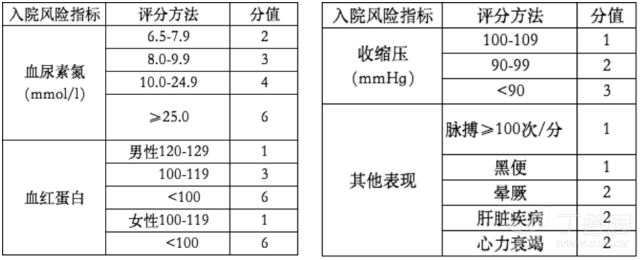
4.抗栓治疗策略的调整
ACS 抗栓治疗过程中一旦发生上消化道出血应综合评估缺血与出血风险
小出血患者,可在充分止血及监测下继续服用抗栓药物
严重出血患者,应考虑减少药物种类及剂量
当出血无法控制或可能威胁生命时,应立即停药,予新鲜血小板输注等治疗
血栓事件高风险的患者(如 BMS 置入 ≤ 1 个月或 DES 置入 ≤ 3 个月),应积极采用内镜下止血治疗,并尽可能保留 DAPT
溃疡性出血复发危险较高的患者,不建议使用氯吡格雷替代阿司匹林,而应该给予阿司匹林联合 PPI 治疗
满足以下条件考虑出血已经得到控制,5d 后可恢复使用抗血小板药物
血流动力学稳定
不输血情况下,血红蛋白稳定
BUN 不继续升高
肠鸣音不活跃
便潜血转阴(非必需条件)
5.选用合适的 PPI 预防及治疗消化道损伤
PPI 明显降低服用阿司匹林和(或)氯吡格雷患者所致消化道损伤的发生率
PPI 是预防抗血小板药物相关消化道损伤的首选药物
高危患者可在抗血小板药物治疗的前 6 个月联合使用 PPI,6 个月后改为 H2RA 或间断服用 PPI
考虑不同 PPI 对氯吡格雷抗血小板作用的影响,建议避免使用对 CYP2CⅠ9 抑制作用强的 PPI,如奥美拉唑和埃索美拉唑
6.出血的处理
(1)2011 ESC 血栓工作组对出血的管理策略如下
发生小出血不需要改变现有的治疗(Ⅰ,C)
发生大出血时,需要中断或中和抗血小板或抗凝治疗,除非出血可以通过其他止血措施确定(Ⅰ,C)
输血可使临床结局恶化,所以需要个体化考虑输血治疗措施,在血流动力学稳定,没有明显出血症状,血球压积>25%,血红蛋白计数>8 g/dl,患者可以使用。(Ⅰ,C)
(2)出血的药物处理
内镜诊断与治疗
内镜检查目的:明确出血的病因和部位、止血治疗,应兼顾缺血、出血及内镜操作的风险
诊断性的内镜检查较为安全,为出血低风险操作
内镜下取活检、行息肉切除术、黏膜切除术、内镜黏膜下剥离术等为出血高危操作
内镜检查时机和治疗策略
缺血风险高危者:推迟内镜下检查或治疗,行相关风险评估,每 24~48 小时评估 1 次是否行内镜检查。根据心脑血管疾病与消化道出血的危险程度,优先处理危及生命的病变
对于缺血风险低危、出血风险较高的患者:内镜操作前应至少停用抗血小板药物 5d,抗凝药可根据其半衰期进行调整。
合并大出血或内镜检查提示为高危(Forrest I-Ⅱb)的患者,应在严密监测及生命体征平稳的条件下于 24~48 h 内行内镜检查(严重出血 12 h 以内),明确诊断和进行必要的干预;内镜下可单独采用热凝或机械方法或与注射方法联合止血。
对于长期使用华法林抗凝的患者,一旦发生出血,应纠正凝血状态,尽快行内镜检查与治疗。
研究显示,当 INR 在 1.5~2.5 时内镜仍可成功止血,而超过 2.7 时则内镜止血后再出血发生率仍较高
在纠正凝血作用的同时给予输血,将 INR 降至 2.5 以下,从而为内镜止血创造条件。
在等待内镜的过程中,可使用促胃肠动力剂和 PPI
(3)再出血的预防与处理(多学科联合決策)
再出血的治疗措施包括
再行内镜止血
经导管动脉栓塞
外科手术
对于无法控制的出血应考虑靶向或经验性经导管动脉栓塞治疗,内镜和放射介入治疗无效需行手术治疗
(4)下消化道出血
影像学检查评估
结肠镜是明确急性下消化道出血病因的主要方法,早期检查能提高出血部位的检出率,但掌握检查时机。
在常规内镜检查未明确病因时,可以采用胶囊内镜及小肠镜检查。
CT 血管造影术(CTA)和放射性核素显像有助于明确出血原因和定位。
钡剂灌肠及结肠双重对比造影应在出血停止后进行。
抗栓药物的调整
止血治疗方案:内镜止血治疗、介入栓塞治疗、外科手术治疗

